AMR
目標と実績
中長期目標
SHIONOGIでは、2035年度までにSHIONOGIが取り扱うすべての抗菌薬の製造プロセスが英国規格協会BSI(The British Standards Institution)の抗菌薬製造に関する国際認証「BSI Kitemark™ for Minimized Risk of AMR」を取得することを目指しています。これはAMRの発生に配慮し、責任をもって抗菌薬を製造していることを、客観的な第三者評価を通じて保証し、ステークホルダーの皆さまに明確に示すための取り組みです。
また、抗菌薬の製造過程における環境への影響を軽減するために、抗菌薬およびその原薬・中間体を取り扱う自社グループの工場やサプライヤー(表1)に対する監査(AMR監査)およびそのフィードバックを通じて、サプライチェーン全体で抗菌薬環境排出の適正管理を実現することとしています。
AMRに対する取り組み
BSI Kitemark™ for Minimized Risk of AMR 認証取得
SHIONOGIグループの生産グループ会社であるシオノギファーマの金ケ崎工場では、中長期目標に基づき、多剤耐性グラム陰性菌感染症治療薬「セフィデロコル」の原薬製造および製剤工程において、「BSI Kitemark™ for Minimized Risk of AMR」の審査を受けました。その結果、2025年10月、日本の医薬品製造施設として初めて本認証を取得しました。

AMR監査
表1:SHIONOGIが扱う抗菌薬原薬の監査対象
抗菌薬の原薬名 |
製造サイト |
製造工程 |
||
|---|---|---|---|---|
原薬 |
製剤 |
一次包装 |
||
フロモキセフ |
SHIONOGI |
● |
● |
● |
A社(日本) |
|
● |
● |
|
セフカペンピボキシル |
SHIONOGI |
● |
● |
● |
ラタモキセフ |
SHIONOGI |
● |
● |
● |
ドリペネム |
SHIONOGI |
● |
● |
● |
B社(日本) |
|
● |
● |
|
セフィデロコル |
SHIONOGI |
● |
● |
● |
I社(イタリア) |
● |
|
● |
|
スルファメトキサゾール |
C社(日本) |
|
● |
● |
F社(インド |
● |
|
|
|
G社(インド) |
● |
|
||
メトロニダゾール |
D社(日本) |
|
● |
● |
H社(イタリア) |
● |
|
|
|
E社は現在SHIONOGIと取引がないため削除
*1 AMR Industry Alliance(外部リンク)
2016年9月に開催されたダボス会議において、12社のリーディングカンパニーとともに、“AMR Industry Roadmap”に署名しました。署名企業は、率先して自社グループおよび委託先の管理を行うことと、AMR対策のロードマップを定め、その環境排出の管理手法をすべての抗菌薬製造メーカーに提供することなどを通じて、AMRの発生抑制を目指しています。本活動は、現在“AMR Industry Alliance”として抗菌薬を扱う多くの会社も加えた活動に発展しています。

*2 Antibiotic Manufacturing Standard(外部リンク)
2025年5月にStandardが改定され、これまで対象工程としていた製薬および製剤に加え、新たに一次包装工程が追加されました。これに伴い、2026年度以降のAMR監査の計画を立案する際には、一次包装工程のみを委託しているサプライヤーも監査対象に含める予定です。
表2:サプライヤーの監査結果(2024年度までの実績)
サプライヤー名 |
マネジメント |
排水管理 |
固形廃棄物管理 |
環境排出基準値の |
|---|---|---|---|---|
A社 |
〇 |
〇 |
〇 |
〇 |
B社 |
〇 |
〇 |
〇 |
〇 |
C社 |
〇 |
〇 |
〇 |
〇 |
D社 |
〇 |
〇 |
〇 |
△ |
F社 |
〇 |
〇 |
〇 |
〇 |
G社 |
〇 |
△ |
〇 |
△ |
H社 |
〇 |
〇 |
〇 |
〇 |
I社 |
〇 |
〇 |
〇 |
〇 |
E社は現在SHIONOGIと取引がないため削除
○:「Standard」の基準に適合
△:「Standard」の基準と比べ、一部不適合があり、是正処置対応中
×:「Standard」の基準と比べ、複数の不適合があり、是正処置対応中
抗菌薬の排出抑制・管理の取り組み
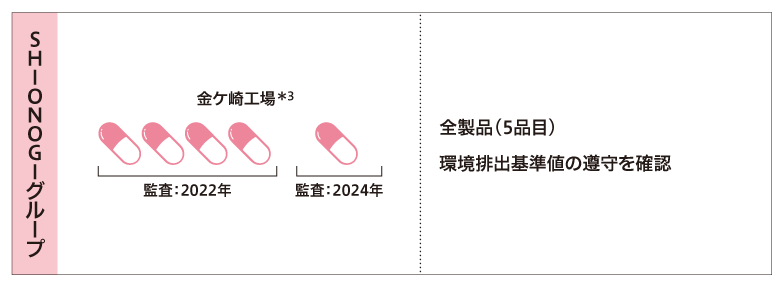
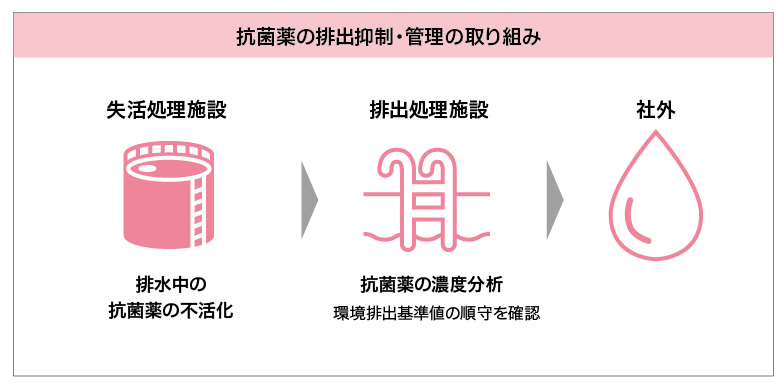
SHIONOGIにおける抗菌薬製造の旗艦工場である金ケ崎工場では、抗菌薬の排出抑制および管理の一環として、製造棟ごとに製造過程で発生する排水中の抗菌薬の不活化処理を実施しています。不活化処理を施した排水は、事業所内の排水処理施設を経由して排出しています。
また、AMRIAのStandardに基づき、毎年事業所からの排水に含まれる抗菌薬濃度を評価しており、現在金ケ崎工場で製造している5品目すべての抗菌薬について、排水中の濃度が自然環境に排出しても影響のない「環境排出基準値*4」以下であることを確認しています。濃度評価には、高速液体クロマトグラフィー法(HPLC)による直接測定に加え、製造量や排水量などのデータをもとに算出するマスバランス法も併用しています。
万が一、異常が認められた場合には、排水を緊急避難槽に一時的に回避し、原則として回収処理を行うことで、自然環境への排出を防止する運用を徹底しています。
抗菌薬製造プロセスから発生する固形廃棄物については、回収のうえ、外部の専門業者に委託し焼却処分しており、固形廃棄物を介して抗菌薬が環境中に排出されることはありません。
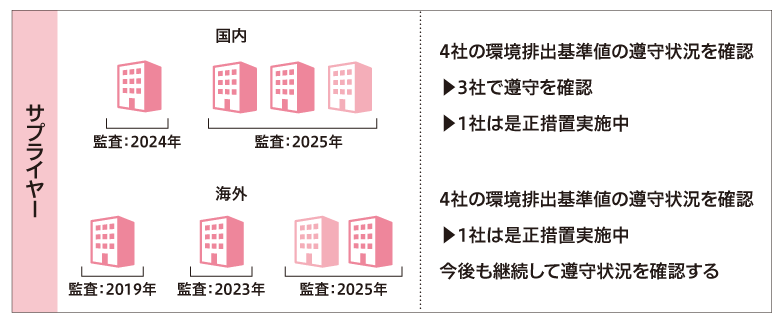
サプライヤーに製造を委託している抗菌薬については、AMR監査の結果として、国内の4社で製造している抗菌薬4品目のうち、3社3品目で環境排出基準値の遵守が確認されました。遵守が確認できなかった1社1品目については、現在是正措置を実施しています。同様に、海外の4社で製造している抗菌薬4品目のうち、3社3品目で環境排出基準値の遵守が確認されており、1社1品目については是正措置を進めています。今後も国内外のサプライヤーに対してAMR監査を継続的に実施し、環境排出基準の遵守状況を確認していく予定です。
One Health – AMR and the environmentへの登壇
2024年6月、BSIが主催するwebinarイベント「One Health – AMR and the environment」において、Shionogi Inc.のGareth Morgan (Global Head, Portfolio Management and AMR Policy)がパネリストとして登壇しました。抗菌薬製造メーカーやサプライヤーなどの聴講者に向けて、SHIONOGIの抗菌薬製造工場における排出抑制・管理の取り組みや、関連サプライヤーに対するAMR監査の実施状況などについて説明しました。