グローバル開発体制
SHIONOGIのグローバル開発体制
安全かつ迅速に質の高い開発をグローバルに展開していくために、日本に本部を置くSHIONOGIでは、米国のShionogi Inc.と欧州のShionogi B.V.との間で「グローバル開発ポリシー」を共有し、開発本部組織のグローバル化を進めています。
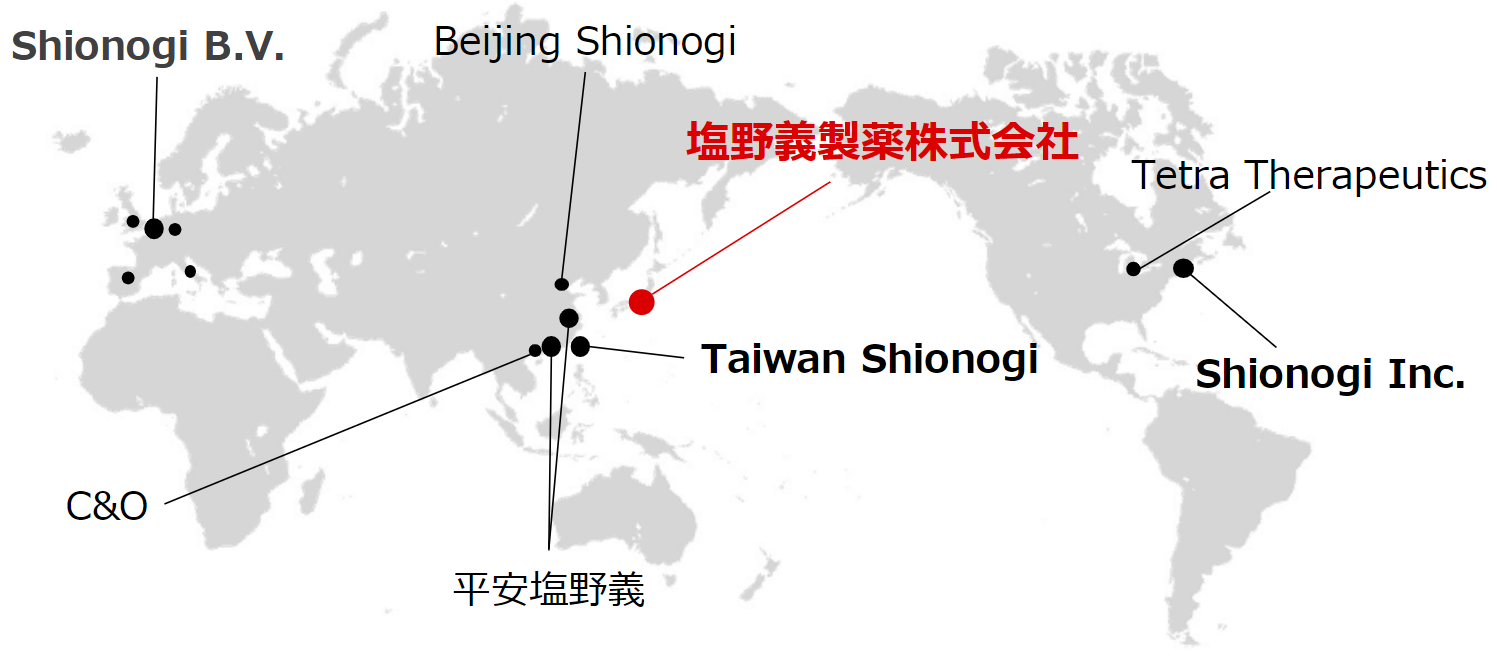
国際共同治験が多くなる中、日本の国内開発本部が世界各拠点の中心となり、開発プロジェクトをリードし,安全で,質の高い臨床試験を推進していきます。
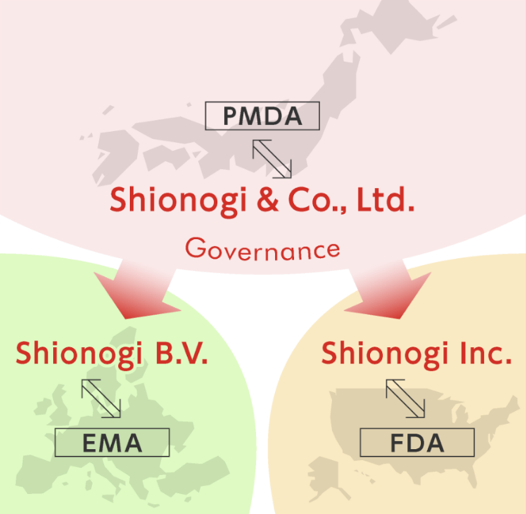
Shionogi & Co., Ltd
日本の大阪に拠点を置くグローバル開発体制の本部。患者様が必要とする医療用製品の安全性・有効性を的確に評価するための開発計画を立案します。
日本の医薬品医療機器総合機構(PMDA)と治験の相談をするとともに各地域担当者を通して申請国の規制当局が治験を実施するために必要とする要件を確認し、グローバルで治験を実装できる体制を整えています。

Shionogi Inc.
米国ニュージャージー州から世界最大の医薬品市場である米国での自社創製品の開発・販売活動に加え、積極的なライセンス活動により製品ポートフォリオの充実およびその価値最大化に取り組んでいます。
また、海外からの臨床データを日本での申請に使用できるよう、日・米両国の規制に従う臨床試験を日本のにあるHeadquartersShionogiの本部とともに計画設計しています。

Shionogi B.V.
英国、ロンドンに開発拠点を置き、グローバル製品の開発のスピードアップや販売パートナーの選定、さらにはアカデミアとの共同研究を中心とした産学連携プログラム「SHIONOGI Science Program」の推進において重要な役割を果たし、当社製品の欧州市場への迅速な上市を進めてまいります。

