おしらせ
2026/02/24
塩野義製薬と日立、生成AIを活用した医薬品開発の規制関連文書作成支援ソリューションを提供開始
塩野義製薬株式会社(代表取締役会長兼社長CEO:手代木 功、以下、「塩野義製薬」または「当社」)は、当社が保有する生成AIを活用した医薬品開発に関する規制関連文書の作成支援ソリューション(以下、「本ソリューション」)について、株式会社日立製作所(執行役社長兼CEO:德永 俊昭、以下「日立」)へライセンス提供する契約を締結しました。本契約に基づき、日立は2026年2月から日本国内で医薬品・ヘルスケア企業向けに本ソリューションの提供を開始しました。
規制関連文書の作成支援ソリューションの概要
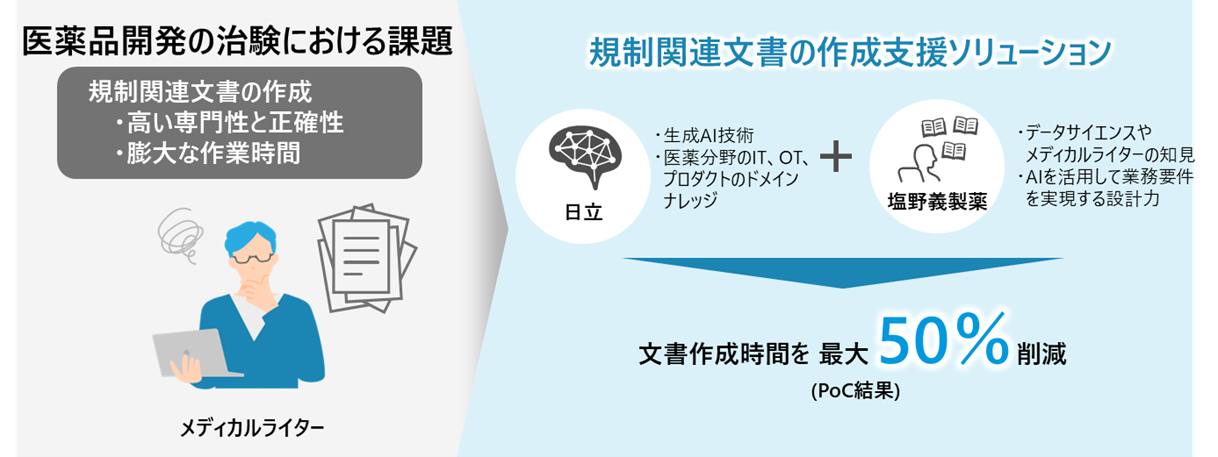
医薬品開発では、治験実施計画書や治験総括報告書などの規制関連文書の作成に通常3~5カ月を要し、文書作成の中心的な役割を担うメディカルライターを中心に膨大な作業負荷が伴います。この業務効率の向上は、医薬品開発スピードを左右する重要な課題となっています。こうした課題に対応するため、塩野義製薬は、医薬品・ヘルスケア業界の課題を解決するDXサービス創出に向けた日立との業務提携*1のもと、本ソリューションの開発を進めてきました。
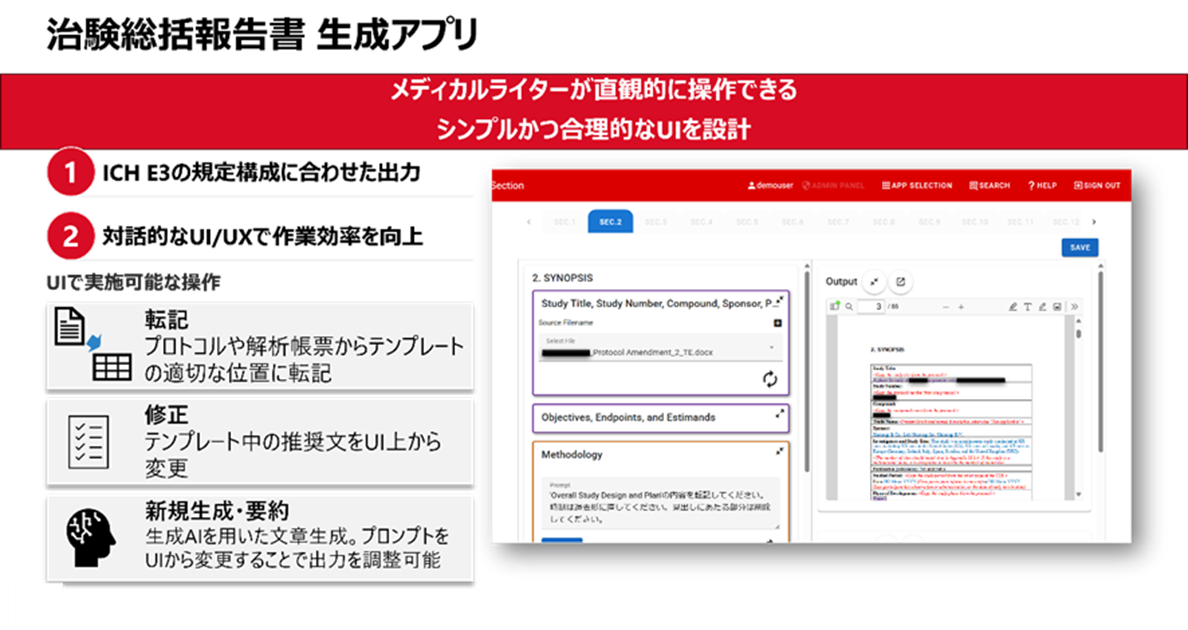
本ソリューションは、当社メディカルライターの専門知識や実務経験、データサイエンティストのデータ活用力とAI設計力に、日立の生成AI活用ノウハウを結集して開発したものです。現場の業務フローを的確に反映した設計により、導入直後から実務で活用でき、日本語・英語が混在する膨大な治験データから要点を抽出し、規制関連文書の初稿を自動生成します。これにより文書作成プロセスを大幅に効率化し、医薬品開発のスピード向上と現場業務の負担軽減に貢献します。当社で実施したPoC(概念実証)では、治験総括報告書*2の作成時間を約50%、治験実施計画書*3の作成時間を約20%削減する効果を確認しました。
*1 2025年1月22日、日立・塩野義製薬ニュースリリース「塩野義製薬と日立、データと生成AIなどを活用した」革新的な医薬品・ヘルスケア業界向けサービス創出に向けた業務提携を開始 https://www.hitachi.co.jp/New/cnews/month/2025/01/0122.html
*2 治験の目的、方法、対象、評価項目などを定めた基本文書であり、治験の適正かつ安全な実施を保証する
*3 治験終了後に作成される報告書で、試験結果や解析、結論をまとめ、薬事申請や評価に用いられる重要な資料
塩野義製薬は、取り組むべきマテリアリティ(重要課題)の一つとして「イノベーションの創出」を特定し、「新たなプラットフォームでヘルスケアの未来を創り出す」というSHIONOGI Group Visionのもと、ヘルスケア領域における技術革新と社会実装を推進しています。塩野義製薬と日立は、生成AIを活用した本ソリューションの提供を通じて、医薬品業界の生産性向上と開発期間短縮を進め、より早く医薬品を患者さまに届ける業界モデルケースの創出を目指してまいります。
以 上
■塩野義製薬について
塩野義製薬は、従来の医療用医薬品を中心に提供する「創薬型製薬企業」から、ヘルスケアサービスを提供する「HaaS企業」へ変革することを掲げています。当社は、これまで培った創薬型製薬企業としての強みを磨きつつ、外部パートナーとの連携を含めた取り組みを強化し、社会に対して新たな価値を提供し続けていくことで、患者さまや社会の抱える困り事の解決に取り組んでまいります。
詳しくは、塩野義製薬のウェブサイト(https://www.shionogi.com/jp/ja/)をご覧ください。
■日立製作所について
日立は、IT、OT(制御・運用技術)、プロダクトを活用した社会イノベーション事業(SIB)を通じて、環境・幸福・経済成長が調和するハーモナイズドソサエティの実現に貢献します。デジタルシステム&サービス、エナジー、モビリティ、コネクティブインダストリーズの4セクターに加え、新たな成長事業を創出する戦略SIBビジネスユニットの事業体制でグローバルに事業を展開し、Lumadaをコアとしてデータから価値を創出することで、お客さまと社会の課題を解決します。2024年度(2025年3月期)売上収益は9兆7,833億円、2025年3月末時点で連結子会社は618社、全世界で約28万人の従業員を擁しています。詳しくは、www.hitachi.co.jpをご覧ください。
[お問合せ先]
塩野義製薬ウェブサイト お問い合わせフォーム:
